Inmunología Humana
-
INTRODUCCIÓN AL SISTEMA INMUNE HUMANOIntroducción. Conceptos básicos10 Temas
-
Introducción Inmunología
-
Funciones sistema inmune y barreras de defensa
-
Inmunidad innata vs adaptativa
-
Respuesta humoral vs celular
-
Respuesta adaptativa primaria vs secundaria
-
Características de la respuesta inmunitaria adaptativa
-
Concepto de antígeno
-
La respuesta inmunitaria específica es clonal
-
Revisión de los componentes del sistema inmunitario
-
Patología general del sistema inmunitario
-
Introducción Inmunología
-
Células del sistema inmune y diferenciación celular6 Temas
-
Hematopoyesis
-
Las células sanguíneas (I): Granulocitos y Mastocitos
-
Las células sanguíneas (II): Plaquetas, Eritrocitos, Monocitos y Macrófagos
-
Las células sanguíneas (III): Linfocitos (T y B), Células plasmáticas y LGL (Linfocitos NK)
-
Las células sanguíneas (IV): Células dendríticas y proporciones relativas de los tipos celulares
-
Funciones y gestión de receptores para antígenos
-
Hematopoyesis
-
Tejidos del sistema inmune: órganos linfoides 1º y 2º3 Temas
-
Células y mecanismos de la inmunidad innata (I): macrófagos, receptores y mecanismos efectores5 Temas
-
Células y mecanismos de la inmunidad innata (II): linfocitos NK, receptores y mecanismos efectores4 Temas
-
MOLÉCULAS IMPLICADAS EN EL RECONOCIMIENTO DE ANTÍGENOEl receptor de antígeno del linfocito B6 Temas
-
Inmunoglobulinas (I): Formas en la naturaleza, estructura y dominio básico
-
Inmunoglobulinas (II): Clases, formas, variabilidad y tejidos
-
Inmunoglobulinas (III): Enlaces antígeno-anticuerpo y funciones
-
Inmunoglobulinas (IV): Receptores para inmunoglobulinas
-
Inmunoglobulinas (V): Procesamiento de RNA, receptor del linfocito B, complejo co-receptor y activación célula B
-
Inmunoglobulinas (VI): Desarrollo / Diferenciación células B
-
Inmunoglobulinas (I): Formas en la naturaleza, estructura y dominio básico
-
El receptor de antígeno del linfocito T4 Temas
-
Mecanismos de generación de la diversidad de linfocitos T y B9 Temas
-
Genes para las cadenas pesadas y ligeras: Diversidad potencial
-
Reordenamiento de los genes
-
Mecanismos de amplificación de la diversidad
-
Expresión de las inmunoglobulinas en el BCR
-
Maduración de los linfocitos B
-
La cooperación T-B
-
Anomalías/Problemas en el proceso (CLÍNICA)
-
Maduración de los linfocitos B
-
Variabilidad en el repertorio del TcR en linfocitos T
-
Genes para las cadenas pesadas y ligeras: Diversidad potencial
-
El complejo principal de histocompatibilidad (I): estructura proteica, genética y nomenclatura3 Temas
-
El complejo principal de histocompatibilidad (II): Procesamiento y presentación de antígeno, polimorfismo y aplicaciones clínicas5 Temas
-
MOLÉCULAS ACCESORIAS DE LA RESPUESTA INMUNEEl sistema del complemento y sus receptores (I): vía clásica y vía alternativa4 Temas
-
El sistema del complemento y sus receptores (II): vía de las lectinas, vía lítica y regulación3 Temas
-
Moléculas implicadas en la comunicación intercelular (I): citocinas y sus receptores5 Temas
-
Moléculas implicadas en la comunicación intercelular (II): moléculas de adhesión y sus ligandos3 Temas
-
EL SISTEMA INMUNE EN ACCIÓN BLOQUEGeneración de linfocitos T efectores4 Temas
-
Generación de linfocitos B efectores7 Temas
-
Sistema Inmune asociado a mucosas (MALT)9 Temas
-
Introducción MALT
-
Estructura del tejido linfoide asociado a la mucosa intestinal
-
Recirculación y migración selectiva de linfocitos al intestino
-
Barrera epitelial intestinal: Función Inmunológica
-
Receptores para el reconocimiento de patrones moleculares
-
Inmunoglobulinas Poliméricas: IgM + IgA
-
Vías de entrada del antígeno en el intestino
-
Diferenciación de los linfocitos T efectores MALT
-
Tolerancia Oral ante antígenos solubles
-
Introducción MALT
-
La respuesta inmune (I): inmunidad innata e inflamación aguda8 Temas
-
Barreras no específicas frente a infección por microorganismos patógenos
-
Principales leucocitos que paticipan en las inmunidad innata
-
La rección inflamatoria
-
Inflamación aguda
-
Sucesos del proceso inflamatorio
-
Citocinas producidas por macrófagos: efectos locales y sistémicos
-
Efectos de las citocinas en la inmunidad innata
-
Proteínas de fase aguda
-
Barreras no específicas frente a infección por microorganismos patógenos
-
La respuesta inmune (II): mecanismos de la inmunidad específica8 Temas
-
La respuesta inmune (III): respuesta frente a virus, bacterias y hongos, protozoos y helmintos9 Temas
-
Principales enfermedades infecciosas mortales
-
Patógenos infecciosos
-
Respuestas frente a bacterias extracelulares
-
Respuesta frente a bacterias intracelulares
-
Proceso de fagocitosis
-
Respuestas frente a protozoos y helmintos
-
Ciclo vital del plasmodium
-
Respuestas inmunitarias frente a virus
-
Mecanismos de evasión inmunitaria. Virales y bacterianos.
-
Principales enfermedades infecciosas mortales
-
REGULACIÓN e INTRODUCCIÓN A LA INMUNOPATOLOGÍARegulación de la respuesta inmune (I): regulación por moléculas8 Temas
-
Regulación de la respuesta inmune: Introducción
-
Regulación por moléculas: el complemento (I)
-
Proteínas reguladoras del complemento y proceso de regulación (II)
-
Proceso de regulación por complemento (III)
-
Regulación de los anticuerpos preformados
-
Regulación por anticuerpos: Redes idiotípicas
-
Regulación por moléculas de linfocitos T
-
Regulación a nivel bioquímico: ITAM frente a ITIM
-
Regulación de la respuesta inmune: Introducción
-
Regulación de la respuesta inmune (II): regulación por células y sistemas4 Temas
-
El sistema inmune a lo largo del ciclo vital: Inmunosenescencia6 Temas
-
Introducción a la inmunopatología13 Temas
-
Conceptos básicos
-
Inmunodeficiencias
-
Las Inmunodeficiencias (II): Déficits de Complemento
-
Las Inmunodeficiencias (III): Déficits de citocinas en receptores
-
Las Inmunodeficiencias (IV): Déficits de TLR's
-
Las Inmunodeficiencias (V): Déficits de función fagocitaria
-
Las Inmunodeficiencias (VI): Déficit de linfocitos B
-
Las Inmunodeficiencias (VII): Déficits de linfocitos T
-
Inmunodeficiencias primarias (IDP's): Clínica y Diagnóstico
-
Hipersensibilidades
-
Autoinmunidad
-
Trasplantes. Rechazo
-
Inmunidad frente a tumores
-
Conceptos básicos
-
Introducción a la Inmunoterapia8 Temas
-
Vacunas (I): Bases inmunológicas
-
Vacunas (II): Tipos de vacunas
-
Inmunoterapia frente a enfermedades autoinmunes
-
Anticuerpos monoclonales en la terapia del cáncer
-
Otras estrategias anti-tumorales
-
Tratamiento “clásico” de la patología alérgica
-
Inmunoterapia en el trasplante de órganos
-
Tratamiento de inmunodeficiencias primarias
-
Vacunas (I): Bases inmunológicas
Reguladores del sistema de complemento (II)
Aquí tienes el temario explicado en el vídeo anterior. Si tienes alguna duda plantéala en el sistema de comentarios del final de la página.
Regulación del sistema de complemento
Dados los devastadores efectos destructivos que desencadena el sistema de complemento, y la forma en que su activación es rápidamente disparada y amplificada, no es sorprendente que existan múltiples mecanismos que impidan su activación descontrolada.
Un mecanismo pasivo de regulación del sistema de complemento es la labilidad de algunos de sus componentes, que permite una desactivación espontánea de los mismos cuando no son estabilizados en una reacción con otros componentes. Por ejemplo, la convertasa de C3 de la vía alternativa tiene una vida media activa de unos 5 minutos, a menos que sea estabilizada por la properdina.
Los mecanismos activos de regulación del sistema del complemento incluyen a un conjunto de proteínas reguladoras que desactivan diferentes elementos del complemento. Las proteínas reguladoras del complemento pueden encontrarse en forma soluble o ancladas a la membrana, como se detalla en la Figura 12.8.
Es necesario distinguir entre los receptores de complemento y las proteínas reguladoras del complemento que tapizan las membranas celulares. En ambos casos sus ligandos son componentes del complemento, pero las funciones biológicas de unos y otras difieren: los primeros sirven a las células del sistema inmunitario para mejorar la eliminación de patógenos, las segun- das inhiben la activación descontrolada del complemento sobre los tejidos sanos. Hay una excepción: CR1 hace ambas cosas.

(Reproducido de Regueiro J.R., López C., González S. & Martínez E. (2011) Inmunología. Biología y Patología del Sistema Inmune. (4ª Ed.) Editorial Médica Panamericana, Madrid.)
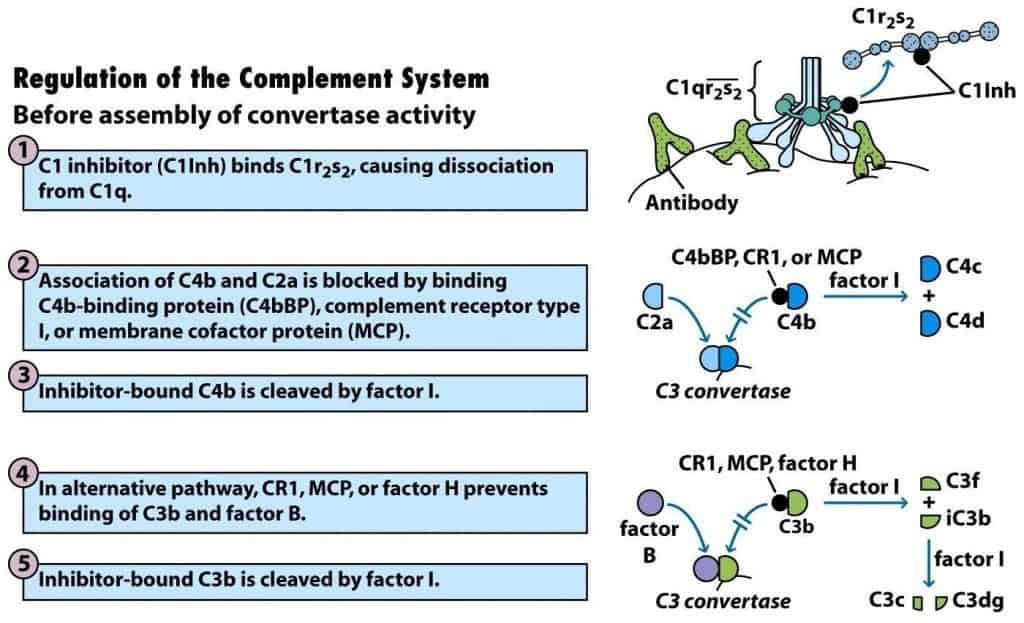
Regulación del complemento antes del ensamblaje de la convertasa
C1 inhibidor (C1Inh) es una glucoproteína soluble capaz de formar un complejo con C1r2s2, produciendo la disociación de C1q e impidiendo, por tanto, la activación de C4 o C2 (Figura 12.9-1).
La reacción catalizada por la convertasa de C3 procedente de cualquiera de las vías de activación es capaz de generar cientos de moléculas de C3b. Estas, a su vez, son capaces de unirse a células cercanas y dañarlas al inducir sobre ellas la formación del MAC. Como mecanismo de regulación, C3b sufre hidrólisis espontánea en el momento que se aleja más de 40 nm de las convertasas de C3. Adicionalmente, existen una serie de proteínas, denominadas RCA (regulators of complement activation), que regulan la actividad de las convertasas de C3. Entre ellas se encuentran la proteína unidora de C4b (C4bBP), el receptor del complemento 1 (CR1) y la proteína cofactor de membrana (MCP). Cada una de estas proteínas reguladoras se une a C4b e impidiendo su unión a C2b. Tras ello, otra proteína reguladora, el factor I, escinde C4b en C4d unida y C4c soluble (Figura 12.9-2,3).
Una secuencia reguladora similar impide el ensamblaje de la convertasa de C3 de la vía alterna. En este caso, CR1, MCP o un componente regulador denominado factor H se unen a C3b e impiden su unión al factor B. A continuación, el factor I escinde C3b en un fragmento iC3b unido y un fragmento C3f soluble. La proteólisis posterior de iC3b por el factor I da lugar a C3c soluble y C3dg unido a la membrana (Figura 12.9-4,5).
(Reproducido de Kindt T.J., Goldsby R.A., Osborne B.A. & Palacios R. (2007) Inmunología de Kuby (6ª Ed.) McGraw-Hill Interamericana, Madrid.)
Regulación del complemento después del ensamblaje de la convertasa
Las proteínas RCA, particularmente C4bBP, CR1 y el factor H, actúan también sobre la convertasa de C3 ensamblada y dan lugar a su disociación. El factor acelerador de la degradación (DAF) o CD55, una glucoproteína de membrana, tiene también la capacidad de disociar la convertasa de C3. Tras la disociación de la convertasa de C3, el factor I escinde el componente C4b o C3b unido a la membrana restante, desactivando irreversiblemente la convertasa (Figura 12.10).

(Reproducido de Kindt T.J., Goldsby R.A., Osborne B.A. & Palacios R. (2007) Inmunología de Kuby (6ª Ed.) McGraw-Hill Interamericana, Madrid.)
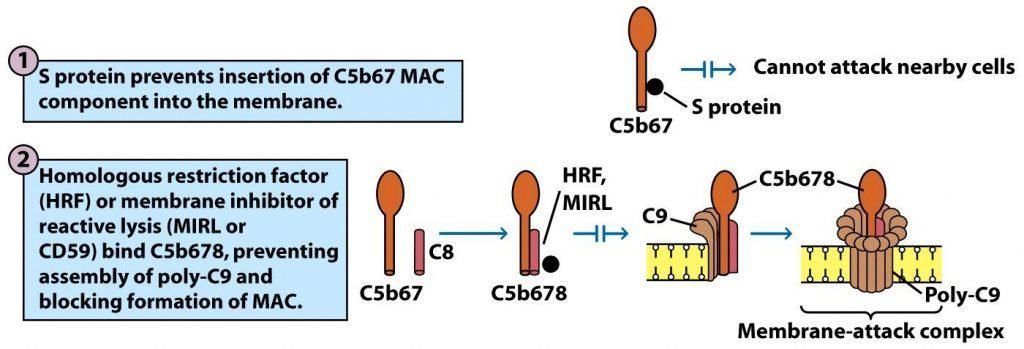
Regulación del complemento en el ensamblaje del MAC
La formación del complejo C5b67 implica un elevado riesgo de lisis para las células del huésped sanas. Por ello, existen múltiples proteínas séricas que contrarrestan esta amenaza, uniéndose al complejo e impidiendo su inserción de la membrana de las células cercanas. Así, la proteína S es capaz de unirse a C5b67 e impedir su inserción en la membrana celular (Figura 12.11-1).
La lisis celular mediada por el complemento es más eficiente cuando el complemento procede de una especie distinta a la de las células que se lisan. Este fenómeno se atribuye al denominado factor de restricción homólogo (HRF), inhibidor de membrana de lisis reactiva (MIRL), CD59 o protectina. Esta proteína se encuentra en la membrana de muchos tipos celulares y protege a las células de la lisis inespecífica mediada por el complemento mediante su unión a C8, con lo que impide el ensamblaje de poli-C9 y su inserción en la membrana. Esta inhibición solo acontece cuando los componentes del complemento proceden de la misma especie que las células diana (Figura 12.11-2).
(Reproducido de Kindt T.J., Goldsby R.A., Osborne B.A. & Palacios R. (2007) Inmunología de Kuby (6ª Ed.) McGraw-Hill Interamericana, Madrid.)

Responses