Inmunología Humana
-
INTRODUCCIÓN AL SISTEMA INMUNE HUMANOIntroducción. Conceptos básicos10 Temas
-
Introducción Inmunología
-
Funciones sistema inmune y barreras de defensa
-
Inmunidad innata vs adaptativa
-
Respuesta humoral vs celular
-
Respuesta adaptativa primaria vs secundaria
-
Características de la respuesta inmunitaria adaptativa
-
Concepto de antígeno
-
La respuesta inmunitaria específica es clonal
-
Revisión de los componentes del sistema inmunitario
-
Patología general del sistema inmunitario
-
Introducción Inmunología
-
Células del sistema inmune y diferenciación celular6 Temas
-
Hematopoyesis
-
Las células sanguíneas (I): Granulocitos y Mastocitos
-
Las células sanguíneas (II): Plaquetas, Eritrocitos, Monocitos y Macrófagos
-
Las células sanguíneas (III): Linfocitos (T y B), Células plasmáticas y LGL (Linfocitos NK)
-
Las células sanguíneas (IV): Células dendríticas y proporciones relativas de los tipos celulares
-
Funciones y gestión de receptores para antígenos
-
Hematopoyesis
-
Tejidos del sistema inmune: órganos linfoides 1º y 2º3 Temas
-
Células y mecanismos de la inmunidad innata (I): macrófagos, receptores y mecanismos efectores5 Temas
-
Células y mecanismos de la inmunidad innata (II): linfocitos NK, receptores y mecanismos efectores4 Temas
-
MOLÉCULAS IMPLICADAS EN EL RECONOCIMIENTO DE ANTÍGENOEl receptor de antígeno del linfocito B6 Temas
-
Inmunoglobulinas (I): Formas en la naturaleza, estructura y dominio básico
-
Inmunoglobulinas (II): Clases, formas, variabilidad y tejidos
-
Inmunoglobulinas (III): Enlaces antígeno-anticuerpo y funciones
-
Inmunoglobulinas (IV): Receptores para inmunoglobulinas
-
Inmunoglobulinas (V): Procesamiento de RNA, receptor del linfocito B, complejo co-receptor y activación célula B
-
Inmunoglobulinas (VI): Desarrollo / Diferenciación células B
-
Inmunoglobulinas (I): Formas en la naturaleza, estructura y dominio básico
-
El receptor de antígeno del linfocito T4 Temas
-
Mecanismos de generación de la diversidad de linfocitos T y B9 Temas
-
Genes para las cadenas pesadas y ligeras: Diversidad potencial
-
Reordenamiento de los genes
-
Mecanismos de amplificación de la diversidad
-
Expresión de las inmunoglobulinas en el BCR
-
Maduración de los linfocitos B
-
La cooperación T-B
-
Anomalías/Problemas en el proceso (CLÍNICA)
-
Maduración de los linfocitos B
-
Variabilidad en el repertorio del TcR en linfocitos T
-
Genes para las cadenas pesadas y ligeras: Diversidad potencial
-
El complejo principal de histocompatibilidad (I): estructura proteica, genética y nomenclatura3 Temas
-
El complejo principal de histocompatibilidad (II): Procesamiento y presentación de antígeno, polimorfismo y aplicaciones clínicas5 Temas
-
MOLÉCULAS ACCESORIAS DE LA RESPUESTA INMUNEEl sistema del complemento y sus receptores (I): vía clásica y vía alternativa4 Temas
-
El sistema del complemento y sus receptores (II): vía de las lectinas, vía lítica y regulación3 Temas
-
Moléculas implicadas en la comunicación intercelular (I): citocinas y sus receptores5 Temas
-
Moléculas implicadas en la comunicación intercelular (II): moléculas de adhesión y sus ligandos3 Temas
-
EL SISTEMA INMUNE EN ACCIÓN BLOQUEGeneración de linfocitos T efectores4 Temas
-
Generación de linfocitos B efectores7 Temas
-
Sistema Inmune asociado a mucosas (MALT)9 Temas
-
Introducción MALT
-
Estructura del tejido linfoide asociado a la mucosa intestinal
-
Recirculación y migración selectiva de linfocitos al intestino
-
Barrera epitelial intestinal: Función Inmunológica
-
Receptores para el reconocimiento de patrones moleculares
-
Inmunoglobulinas Poliméricas: IgM + IgA
-
Vías de entrada del antígeno en el intestino
-
Diferenciación de los linfocitos T efectores MALT
-
Tolerancia Oral ante antígenos solubles
-
Introducción MALT
-
La respuesta inmune (I): inmunidad innata e inflamación aguda8 Temas
-
Barreras no específicas frente a infección por microorganismos patógenos
-
Principales leucocitos que paticipan en las inmunidad innata
-
La rección inflamatoria
-
Inflamación aguda
-
Sucesos del proceso inflamatorio
-
Citocinas producidas por macrófagos: efectos locales y sistémicos
-
Efectos de las citocinas en la inmunidad innata
-
Proteínas de fase aguda
-
Barreras no específicas frente a infección por microorganismos patógenos
-
La respuesta inmune (II): mecanismos de la inmunidad específica8 Temas
-
La respuesta inmune (III): respuesta frente a virus, bacterias y hongos, protozoos y helmintos9 Temas
-
Principales enfermedades infecciosas mortales
-
Patógenos infecciosos
-
Respuestas frente a bacterias extracelulares
-
Respuesta frente a bacterias intracelulares
-
Proceso de fagocitosis
-
Respuestas frente a protozoos y helmintos
-
Ciclo vital del plasmodium
-
Respuestas inmunitarias frente a virus
-
Mecanismos de evasión inmunitaria. Virales y bacterianos.
-
Principales enfermedades infecciosas mortales
-
REGULACIÓN e INTRODUCCIÓN A LA INMUNOPATOLOGÍARegulación de la respuesta inmune (I): regulación por moléculas8 Temas
-
Regulación de la respuesta inmune: Introducción
-
Regulación por moléculas: el complemento (I)
-
Proteínas reguladoras del complemento y proceso de regulación (II)
-
Proceso de regulación por complemento (III)
-
Regulación de los anticuerpos preformados
-
Regulación por anticuerpos: Redes idiotípicas
-
Regulación por moléculas de linfocitos T
-
Regulación a nivel bioquímico: ITAM frente a ITIM
-
Regulación de la respuesta inmune: Introducción
-
Regulación de la respuesta inmune (II): regulación por células y sistemas4 Temas
-
El sistema inmune a lo largo del ciclo vital: Inmunosenescencia6 Temas
-
Introducción a la inmunopatología13 Temas
-
Conceptos básicos
-
Inmunodeficiencias
-
Las Inmunodeficiencias (II): Déficits de Complemento
-
Las Inmunodeficiencias (III): Déficits de citocinas en receptores
-
Las Inmunodeficiencias (IV): Déficits de TLR's
-
Las Inmunodeficiencias (V): Déficits de función fagocitaria
-
Las Inmunodeficiencias (VI): Déficit de linfocitos B
-
Las Inmunodeficiencias (VII): Déficits de linfocitos T
-
Inmunodeficiencias primarias (IDP's): Clínica y Diagnóstico
-
Hipersensibilidades
-
Autoinmunidad
-
Trasplantes. Rechazo
-
Inmunidad frente a tumores
-
Conceptos básicos
-
Introducción a la Inmunoterapia8 Temas
-
Vacunas (I): Bases inmunológicas
-
Vacunas (II): Tipos de vacunas
-
Inmunoterapia frente a enfermedades autoinmunes
-
Anticuerpos monoclonales en la terapia del cáncer
-
Otras estrategias anti-tumorales
-
Tratamiento “clásico” de la patología alérgica
-
Inmunoterapia en el trasplante de órganos
-
Tratamiento de inmunodeficiencias primarias
-
Vacunas (I): Bases inmunológicas
Inmunoglobulinas (III): Enlaces antígeno-anticuerpo y funciones
Aquí tienes el temario explicado en el vídeo anterior. Si tienes alguna duda plantéala en el sistema de comentarios del final de la página.
Características de los anticuerpos
La estructura mínima de un antígeno que es reconocida por un anticuerpo y que es capaz de generar una respuesta inmune se denomina epítopo.
Pueden resultar de la consecución de aminoácidos en la estructura primaria (epítopos lineales) o del plegamiento de la proteína (epítopos conformacionales). Los epítopos contactan íntimamente con los parátopos de las inmunoglobulinas.
Las tres características fundamentales de un anticuerpo son la afinidad, la avidez y la especificidad (determinada por la secuencia de aminoácidos de sus dominios variables).
La afinidad determina la rapidez con la que el anticuerpo (Ab) se une al Ag y viene determinada por la fuerza de las uniones entre ambas moléculas. Esta unión nunca será covalente y se encon- trará en un equilibrio desplazado hacia un lado u otro según la afinidad. Esta fuerza de unión y, por tanto, la afinidad, depende del número y tipo de enlaces químicos entre parátopo y epítopo.
Estos enlaces pueden ser de varios tipos (Figura 6.9):
- Puentes de hidrógeno: iones de H compartidos por átomos del Ag y Ab crean cargas parciales opuestas.
- Enlaces electroestáticos: se dan cargas de polaridad opuesta entre Ab y Ag.
- Fuerzas de Van der Waals: fluctuaciones en las nubes de electrones alrededor de moléculas enfrentan átomos vecinos polarizados.
- Enlaces hidrofóbicos: grupos hidrofóbicos del Ab y del Ag se unen excluyendo moléculas de agua.
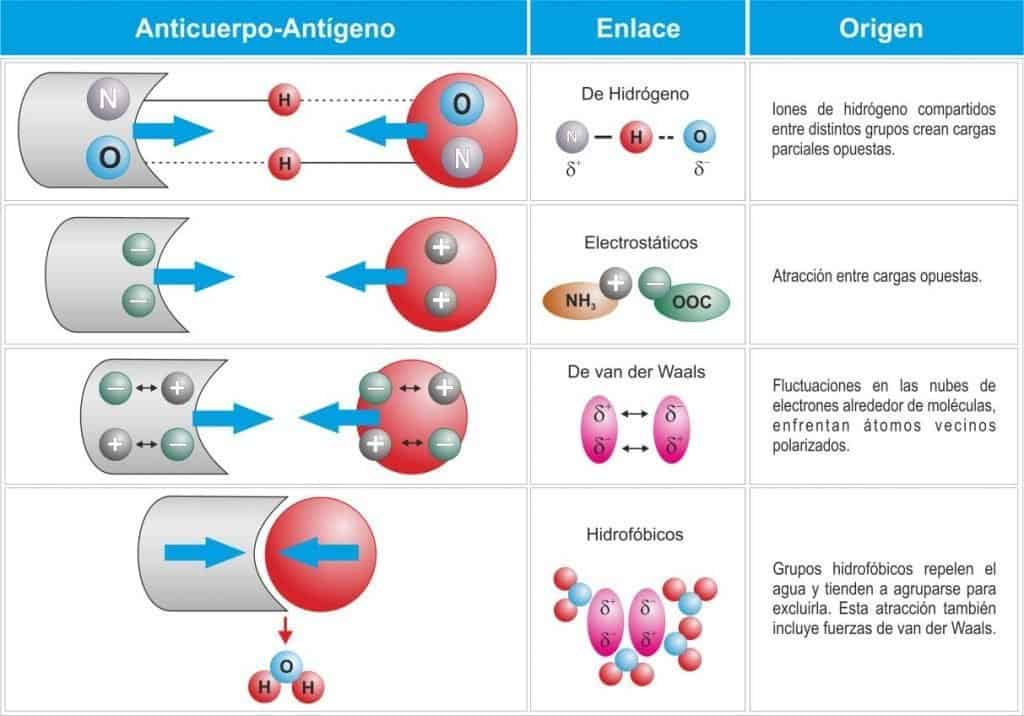
(Reproducido de Regueiro J.R., López C., González S. & Martínez E. (2011) Inmunología. Biolo- gía y Patología del Sistema Inmune. (4ª Ed.) Editorial Médica Panamericana, Madrid.)
Dependiendo del tipo y número de enlaces habrá mayor o menor afinidad de un anticuerpo por su antígeno. La avidez viene dada por el número de sitios de unión. Es la fuerza con la que un anticuerpo multivalente se une a un antígeno multivalente. Hay antígenos con secuencias repetitivas en su estructura. Estos antígenos se comportan de modo multivalente, y la fuerza de unión Ag-Ab es mayor que la simple suma de las afinidades de cada uno de los sitios de unión del anticuerpo al antígeno. Así, a mayor número de sitios de unión, mayor avidez.
Por ejemplo, la IgM pentamérica suele ser la más ávida para un antígeno al presentar 10 sitios de unión. En situaciones fisiológicas, es probable que la avidez sea más importante que la afinidad porque los anticuerpos son mayoritariamente divalentes, y lo más normal es que los antígenos sean multivalentes. La especificidad, la avidez y la afinidad vienen determinadas por la región Fab del anticuerpo. La función es determinada por el fragmento Fc.
Funciones de los anticuerpos
Los anticuerpos son buenos ejemplos de cómo la estructura está íntimamente relacionada con la función. Son moléculas con forma de Y, donde los brazos cortos (Fab) interaccionan con el antígeno y el tallo (Fc) proporciona la funcionalidad efectora. Como consecuencia de la reacción Ab-Ag, se producirán diferentes funciones:
- Aglutinación – neutralización del antígeno. Los anticuerpos son bivalentes, es decir, poseen dos lugares de reconocimiento de antígeno. Esto permite la aglutinación del mismo, para su mejor eliminación. Además, cuando se recubre toda la superficie del patógeno con moléculas de anticuerpos, se produce un fenómeno denominado neutralización. Así, por ejemplo, existen toxinas que atacan a las terminaciones nerviosas, pero cuando los anticuerpos se unen a ellas, las neutralizan.
- Opsonización – fagocitosis. El recubrimiento de la superficie del patógeno por anti- cuerpos, puede tener consecuencias posteriores. Así, los macrófagos, que tienen receptores para la porción cristalizable del anticuerpo (Fc), que se denominan FcR, pueden fagocitar los patógenos que han sido recubiertos por anticuerpo. En este caso, al recubrimiento se le reconoce con el nombre de opsonización.
- Inmovilización del patógeno. Si el anticuerpo se une a la parte móvil del patógeno (cilios, flagelos), va a producir una inmovilización del mismo, reduciendo su patogenicidad.
- Activación del complemento. Al unirse un anticuerpo a un antígeno se produce un cambio conformacional en la región Fc del anticuerpo, que induce la activación del sis- tema del complemento. Sólo son capaces de realizar esta acción la IgM y la IgG, desempeñando una importante función en la inmunidad adaptativa frente a infecciones. La unidad de reconocimiento del sistema del complemento que reconoce los anticuerpos unidos es la proteína C1q del factor C1.
- Expulsión. Cuando las anticuerpos son del tipo IgE y los antígenos son parásitos, la unión IgE-antígeno promueve la liberación de aminas vasoactivas que relajan la musculatura lisa y provocan diarrea en el intestino para expulsar al parásito.
- Citolisis mediada por anticuerpos (ADDC). Otra función que viene mediada por re- ceptores para la porción Fc del anticuerpo es la llamada citotoxicidad mediada por anti- cuerpos (ADCC). Las células efectoras son mayoritariamente los linfocitos NK, que al reconocer el anticuerpo unido a la superficie del patógeno, liberan sustancias citotóxicas que atacan al patógeno. El mecanismo de la ADCC es independiente del sistema complemento y requiere que el linfocito NK exprese receptores de membrana FcR para la porción distal de los anticuerpos IgG (CD16).
- Inmunidad en feto y neonato: durante la gestación y los primeros meses de vida, las inmunoglobulinas maternas son el único mecanismo de defensa específica que tiene el recién nacido. Su sistema inmune no ha madurado aún, y no tiene modo de fabricar sus inmunoglobulinas propias en primera instancia. Estas han de transportarse a través de la placenta, o a través del epitelio intestinal del neonato, procedentes de la leche materna.
Concentración y función de los diferentes isotipos
Cada isotipo de anticuerpo desarrolla más efectivamente alguna de estas funciones efectoras (Figura 6.10). Así, con una misma región variable, diferentes regiones constantes van a llevar asociadas diferencias en la función efectora del anticuerpo:
- IgA: existen dos subclases IgA1 (80-90% del total de IgA del suero) e IgA2 (30-50% del total de IgA de secreciones como la leche). Las dos subclases parecen estar regula- das de forma independiente. Los niveles séricos varían con la edad y se encuentran ele- vados en la mujer durante la lactancia, así como en infecciones crónicas, enfermedades hepáticas y mieloma. Un nivel bajo de IgA indica déficit generalizado de proteínas o inmunodeficiencia específica de IgA. Esta Ig es la más abundante en secreciones seromucosas como la saliva, la leche o el calostro. Forma parte del sistema de defensa de la superficie externa del organismo. En secreciones se presenta en forma de dímero unida a una cadena J, que une los dos monómeros de IgA, y al componente secretor, mientras que en la sangre se presentara en forma de monómero (se compone de dos cadenas alfa pesadas y dos cadenas ligeras). Su función principal es neutralizante aunque también tiene pero en menor medida capacidad de activación del complemento.
- IgD: se encuentra fundamentalmente en plasma (menos de 1% del total de inmunoglobulinas en plasma, e indetectable en individuos sanos) y siempre en forma de monómero. Su función es desconocida pero abunda en la superficie de linfocitos B y se cree que participa en la diferenciación de estas células inducidas por el antígeno. Linfocitos B con IgD se transforma en una célula anérgica (no se va a activar nunca, inútil). También se piensa que puede ser un resto evolutivo que desaparecerá.
- IgE: su concentración plasmática (en forma monomérica) es pequeña y es indetectable en individuos sanos. Se une (mediante receptores para Fc) a la superficie de basófilos y mastocitos y su función es la defensa frente a parásitos grandes, sin embargo en la sociedad industrializada se relaciona con reacciones de hipersensibilidad inmediata, como el asma o la fiebre del heno (hipótesis de higiene).
- IgG: en el plasma o suero de adultos normales la IgG supone el 75% del total de las in- munoglobulinas circulantes. Los niveles séricos de IgG suelen variar con la edad, incluso con la raza. Un nivel elevado de IgG se asocia con enfermedades crónicas del hígado y mieloma; niveles reducidos se pueden asociar con malignidad y graves déficits de proteínas, así como con inmunodeficiencia. Presenta cuatro subclases todas ellas en forma de monómero. IgG1 es la más abundante en plasma mientras que IgG4 la más es- casa. Presenta una gran versatilidad funcional: importante en la inmunidad fetal por atravesar la placenta y entrar en el plasma fetal (único anticuerpo de la etapa neonatal y de origen materno), en respuesta secundaria, en activación del complemento, además de potenciar la fagocitosis, citotoxicidad y neutralización.
- IgM: se encuentra en sangre y en tejidos infectados en forma pentamérica (unidos por cadenas J). Cada unidad consiste en dos cadenas µ pesadas y dos cadenas ligeras. Es el isotipo más importante en la respuesta primaria. Muestra gran eficiencia con antígenos pluripotenciales como bacterias y virus, y actúa en la activación del complemento. Buen anticuerpo neutralizante aunque no tanto como IgG e IgM. Los niveles elevados de IgM se asocian con hepatitis, mieloma, macroglobulinemia de Waldenstrom, infecciones y síndrome de Hiper-IgM (inmunodeficiencia congénita). Los niveles reducidos de IgM se observan en algunas inmunodeficiencias de anticuerpos.
Por tanto en suero encontraremos de mayor a menor abundancia: IgG, IgA, IgM, las cantidades de IgD e IgE serán indetectables en un individuo sano (menos del 1%del total).
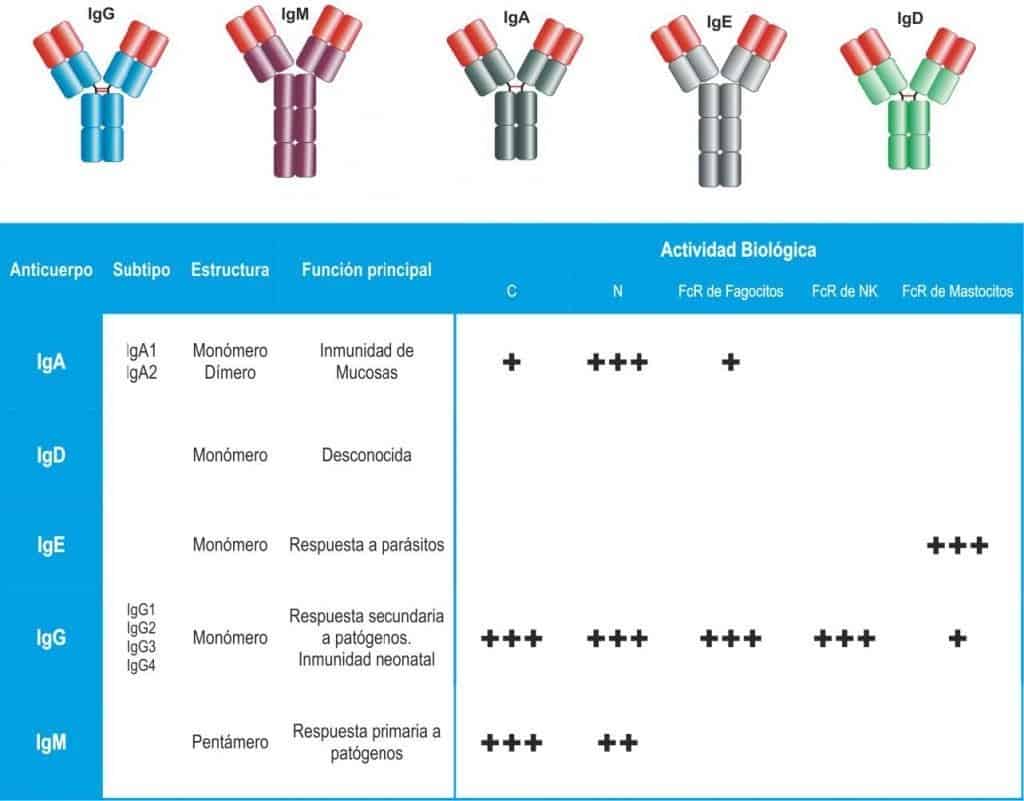
(Reproducido de Regueiro J.R., López C., González S. & Martínez E. (2011) Inmunología. Biología y Patología del Sistema Inmune. (4ª Ed.) Editorial Médica Panamericana, Madrid.)
Salida de IgA a las mucosas
La inmunoglobulina A es el isotipo fundamental en las secreciones, especialmente en los epitlios de los tractos digestivo y respiratorio. Las células plasmáticas (estadío de diferenciación final de linfocitos B) productoras de IgA se encuentran predominantemente en el tejido conectivo (lámina propia) que subyace inmediatamente por debajo de muchas superficies epiteliales.
La IgA sintetizada en la lámina propia se secreta como IgA dimérica asociada a una cadena de unión J (Figura 6.11). Esta forma polimérica de IgA se une selectivamente a un receptor de poliinmunoglobulina (poli-Ig-R) que está presente en las superficies basolaterales de las células epiteliales. Una vez que la IgA dimérica se ha unido a dicho receptor, el complejo se internaliza en la célula y se transporta por el citoplasma de la célula epitelial en vesículas de transporte, hasta la porción apical de la célula. Este proceso se denomina transcitosis.
Una vez en la zona apical de la célula epitelial el receptor de poli-Ig se fragmenta mediante una endoproteasa (favorecida por el pH ácido de la luz intestinal), liberando la porción más externa del receptor todavía unida a la IgA dimérica. Este fragmento del receptor liberado junto a la IgA se denomina componente secretor, y parece que protege a la IgA dimérica de posibles degradaciones enzimáticas, el otro fragmento queda unido a la superficie de la célula epitelial.
Los tejidos con mayor síntesis de IgA son el intestino, el epitelio respiratorio, la mama (en épocas de lactancia) y otras glándulas exocrinas como las salivares y lacrimales. Se cree que la principal función de los anticuerpos IgA es proteger la superficie epitelial de los agentes infec- ciosos, neutralizándolos.
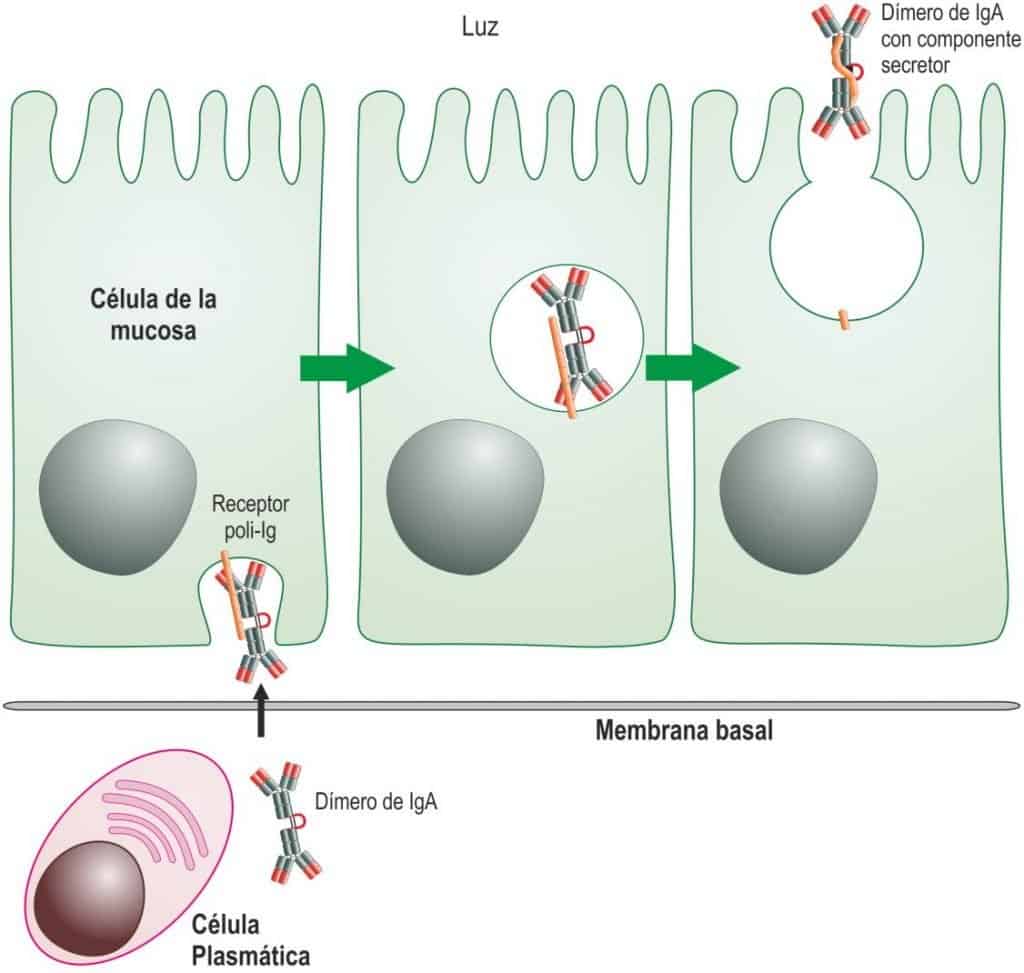
Figura 6.11 Salida de IgA a las mucosas
(Reproducido de Regueiro J.R., López C., González S. & Martínez E. (2011) Inmunología. Biolo- gía y Patología del Sistema Inmune. (4ª Ed.) Editorial Médica Panamericana, Madrid.)

Responses